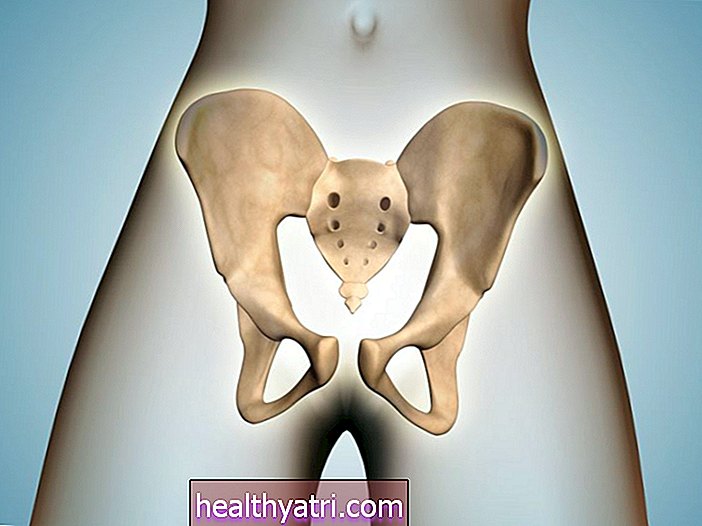
Il virus dell'immunodeficienza umana (HIV) è un retrovirus i cui geni sono codificati con acido ribonucleico (RNA) invece che con acido desossiribonucleico (DNA).
Un retrovirus differisce da un virus tradizionale nel modo in cui infetta, si replica e causa la malattia.
L'HIV è uno dei due soli retrovirus umani della sua classe, l'altro dei quali è il virus T-linfotropico umano (HTLV).
Thana Prasongsin / Getty Images
Cos'è un retrovirus?
HIV e HTLV sono classificati come virus a RNA del gruppo IV della famigliaRetroviridae.Funzionano inserendo il loro materiale genetico in una cellula, quindi modificando la sua struttura e funzione genetica per replicarsi.
L'HIV è ulteriormente classificato come lentivirus, un tipo di retrovirus che si lega a una specifica proteina chiamata CD4.
Retroviridaei virus possonoinfettano mammiferi (compresi gli esseri umani) e uccelli e sono noti per causare disturbi da immunodeficienza e tumori.
La loro caratteristica distintiva è un enzima chiamato trascrittasi inversa, che trascrive l'RNA nel DNA.
Nella maggior parte dei casi, le cellule convertono il DNA in RNA in modo che possa essere trasformato in varie proteine. Ma nei retrovirus, questo processo avviene al contrario (da qui la parte "retro"), dove l'RNA virale viene trasformato in DNA.
Come si infetta l'HIV
L'HIV differisce dall'HTLV in quanto quest'ultimo è un deltaretrovirus. Sebbene entrambi siano caratterizzati dalla trascrizione inversa, i lentivirus si replicano in modo aggressivo, mentre i deltaretrovirus hanno una replicazione attiva minima una volta stabilita l'infezione.
Affinché l'HIV possa infettare altre cellule del corpo, attraversa un ciclo di vita (o replicazione) in sette fasi, che porta a trasformare una cellula ospite in una fabbrica che genera l'HIV. Ecco cosa succede:
- Legame: dopo aver trovato e attaccato una cellula CD4, l'HIV si attacca alle molecole sulla superficie della cellula CD4.
- Fusione: una volta che le cellule sono legate insieme, l'involucro virale dell'HIV si fonde con la membrana cellulare CD4, consentendo all'HIV di entrare nella cellula CD4.
- Trascrizione inversa: dopo che è stato inserito in una cellula CD4, l'HIV rilascia e quindi utilizza un enzima della trascrittasi inversa per convertire il suo RNA in DNA.
- Integrazione: la trascrizione inversa offre all'HIV la possibilità di entrare nel nucleo della cellula CD4, dove, una volta all'interno, rilascia un altro enzima chiamato integrasi, che utilizza per inserire il suo DNA virale nel DNA della cellula ospite.
- Replicazione: ora che l'HIV è integrato nel DNA della cellula CD4 ospite, inizia a utilizzare i macchinari già all'interno della cellula CD4 per creare lunghe catene di proteine, che sono i mattoni per più HIV.
- Assemblaggio: ora, le nuove proteine dell'HIV RNA e dell'HIV prodotte dalla cellula CD4 ospite si spostano sulla superficie della cellula e formano l'HIV immaturo (non infettivo).
- Germogliando: questo HIV immaturo, che non è in grado di infettare un'altra cellula CD4, quindi si fa strada fuori dalla cellula CD4 ospite. Lì, rilascia un altro enzima HIV chiamato proteasi, che rompe le lunghe catene proteiche nel virus immaturo. In tal modo, crea il virus maturo e ora contagioso, che ora è pronto per infettare altre cellule CD4.
Obiettivi per la terapia
Comprendendo i meccanismi di replicazione sopra descritti, gli scienziati sono in grado di mirare e bloccare alcune fasi del ciclo di vita dell'HIV.
Interrompendo la sua capacità di replicarsi, la popolazione virale può essere soppressa a livelli non rilevabili, che è l'obiettivo dei farmaci antiretrovirali per l'HIV.
Attualmente, ci sono nove diverse classi di farmaci antiretrovirali usati per trattare l'HIV, raggruppate in base allo stadio del ciclo di vita che bloccano:
Inibitore di ingresso / allegato
Cosa fanno: si legano a una proteina sulla superficie esterna dell'HIV, impedendo all'HIV di entrare nelle cellule CD4.
Farmaco (i) in questa classe: Fostemsavir
Inibitore post-attaccamento
Cosa fanno: bloccano i recettori CD4 sulla superficie di alcune cellule immunitarie di cui l'HIV ha bisogno per entrare nelle cellule.
Farmaco (i) in questa classe: Ibalizumab-uiyk
Inibitore di fusione
Cosa fanno: impedisce all'HIV di entrare nelle cellule CD4 del sistema immunitario.
Farmaco (i) in questa classe: Enfuvirtide
CCR5 Antagonists
Cosa fanno: bloccano i corecettori CCR5 sulla superficie di alcune cellule immunitarie di cui l'HIV ha bisogno per entrare nelle cellule.
Farmaco (i) in questa classe: Maraviroc
Inibitori nucleosidici della trascrittasi inversa (NRTI)
Cosa fanno: blocca la trascrittasi inversa, un enzima HIV ha bisogno di fare copie di se stesso.
Farmaco (i) in questa classe: Abacavir, emtricitabina, lamivudina, tenofovir disoproxil fumarato, zidovudina
Inibitori non nucleosidici della trascrittasi inversa (NNRTI)
Cosa fanno: si legano e successivamente alterano la trascrittasi inversa, un enzima HIV ha bisogno di fare copie di se stesso.
Farmaco (i) in questa classe: Doravirina, efavirenz, etravirina, nevirapina, rilpivirina
Inibitori della proteasi (PI)
Cosa fanno: blocca la proteasi dell'HIV, un enzima di cui l'HIV ha bisogno per fare copie di se stesso.
Farmaco (i) in questa classe: Atazanavir, darunavir, fosamprenavir, ritonavir, saquinavir, tipranavir
Integrase Strand Transfer Inhibitor (INSTI)
Cosa fanno: blocca l'integrasi dell'HIV, un enzima di cui l'HIV ha bisogno per fare copie di se stesso.
Farmaco (i) in questa classe: Cabotegravir, dolutegravir, raltegravir
Potenziatori farmacocinetici ("booster")
Cosa fanno: utilizzati nel trattamento dell'HIV per aumentare l'efficacia di un medicinale per l'HIV incluso in un regime per l'HIV.
Farmaco (i) in questa classe: Cobicistat
Perché non esiste un farmaco antiretrovirale in grado di fare tutto?
A causa dell'elevata variabilità genetica dell'HIV, è necessaria la terapia antiretrovirale di combinazione per bloccare le diverse fasi del ciclo di vita e garantire una soppressione duratura. Ad oggi, nessun singolo farmaco antiretrovirale è in grado di farlo.
Sfide e obiettivi
I lentivirus si replicano in modo aggressivo, con un tempo di raddoppio di 0,65 giorni durante l'infezione acuta, ma quel processo di replicazione è soggetto a errori. Ciò si traduce in un alto tasso di mutazione, durante il quale più varianti dell'HIV possono svilupparsi in una persona entro un solo giorno.
Molte di queste varianti non sono vitali e non possono sopravvivere. Altri sono vitali e pongono sfide al trattamento e allo sviluppo di vaccini.
Resistenza ai farmaci
Una sfida significativa per trattare efficacemente l'HIV è la capacità del virus di mutare e riprodursi mentre una persona sta assumendo farmaci antiretrovirali.
Questa è chiamata resistenza ai farmaci HIV (HIVDR) e può compromettere l'efficacia delle attuali opzioni terapeutiche e l'obiettivo di ridurre l'incidenza, la mortalità e la morbilità dell'HIV.
HIV di tipo selvaggio
La resistenza ai farmaci dell'HIV può svilupparsi come risultato di qualcosa noto come HIV "wild-type", che è la variante predominante all'interno del pool virale non trattato, grazie al fatto che può sopravvivere quando altre varianti non possono.
La popolazione virale può iniziare a cambiare solo quando una persona inizia a prendere farmaci antiretrovirali.
Poiché l'HIV non trattato si replica così rapidamente e spesso include mutazioni, è possibile che si formi una mutazione in grado di infettare le cellule ospiti e sopravvivere, anche se la persona sta assumendo farmaci antiretrovirali.
È anche possibile che la mutazione resistente ai farmaci diventi la variante dominante e prolifichi. Inoltre, la resistenza può svilupparsi a causa di una scarsa aderenza al trattamento, portando a più resistenza ai farmaci e al fallimento del trattamento.
A volte, quando le persone sono state recentemente infettate dall'HIV, ereditano un ceppo resistente del virus dalla persona che le ha infettate, una cosa chiamata resistenza trasmessa. È anche possibile che qualcuno recentemente infettato erediti una profonda resistenza multi-farmaco a diverse classi di farmaci per l'HIV.
I nuovi trattamenti contro l'HIV offrono una maggiore protezione contro le mutazioni
Laddove alcuni farmaci per l'HIV meno recenti come Viramune (nevirapina) e Sustiva (efavirenz) possono sviluppare resistenza all'HIV con una sola mutazione, i farmaci più recenti richiedono numerose mutazioni prima che si verifichi il fallimento.
Sviluppo di vaccini
Uno degli ostacoli più significativi alla creazione di un vaccino contro l'HIV ampiamente efficace è la diversità genetica e la variabilità del virus stesso. Invece di essere in grado di concentrarsi su un singolo ceppo di HIV, i ricercatori devono tenere conto del fatto che si replica così rapidamente.
Ciclo di replicazione dell'HIV
Il ciclo di replicazione dell'HIV richiede poco più di 24 ore.
E sebbene il processo di replicazione sia veloce, non è il più accurato, producendo ogni volta molte copie mutate, che poi si combinano per formare nuovi ceppi mentre il virus viene trasmesso tra persone diverse.
Ad esempio, nell'HIV-1 (un singolo ceppo di HIV), ci sono 13 sottotipi e sottotipi distinti che sono collegati geograficamente, con una variazione dal 15% al 20% all'interno dei sottotipi e una variazione fino al 35% tra i sottotipi.
Non solo questa è una sfida nella creazione di un vaccino, ma anche perché alcuni dei ceppi mutati sono resistenti all'ART, il che significa che alcune persone hanno mutazioni più aggressive del virus.
Un'altra sfida nello sviluppo di un vaccino è qualcosa chiamato serbatoi latenti, che vengono stabiliti durante la prima fase dell'infezione da HIV e possono effettivamente "nascondere" il virus dalla rilevazione immunitaria, così come gli effetti dell'ART.
Ciò significa che se il trattamento viene interrotto, una cellula infetta in modo latente può essere riattivata, facendo sì che la cellula inizi di nuovo a produrre l'HIV.
Sebbene l'ART possa sopprimere i livelli di HIV, non può eliminare i serbatoi latenti dell'HIV, il che significa che l'ART non può curare l'infezione da HIV.
Sfide dei serbatoi di HIV latenti
Fino a quando gli scienziati non saranno in grado di "pulire" i serbatoi di HIV latenti, è improbabile che qualsiasi vaccino o approccio terapeutico sradichi completamente il virus.
C'è anche la sfida dell'esaurimento immunitario che deriva da un'infezione da HIV a lungo termine. Questa è la graduale perdita della capacità del sistema immunitario di riconoscere il virus e lanciare una risposta appropriata.
Qualsiasi tipo di vaccino contro l'HIV, cura dell'AIDS o altro trattamento deve essere creato tenendo conto dell'esaurimento immunitario, trovando modi per affrontare e compensare le capacità decrescenti del sistema immunitario di una persona nel tempo.
Progressi nella ricerca sui vaccini contro l'HIV
Tuttavia, ci sono stati alcuni progressi nella ricerca sui vaccini, inclusa una strategia sperimentale chiamata "kick-and-kill". Si spera che la combinazione di un agente di inversione della latenza con un vaccino (o altri agenti sterilizzanti) possa avere successo con una strategia sperimentale curativa nota come "kick-and-kill" (alias "shock-and-kill").
Essenzialmente, è un processo in due fasi:
- In primo luogo, i farmaci chiamati agenti di inversione della latenza vengono utilizzati per riattivare l'HIV latente che si nasconde nelle cellule immunitarie (la parte "kick" o "shock").
- Quindi, una volta che le cellule immunitarie vengono riattivate, il sistema immunitario del corpo, o i farmaci anti-HIV, possono colpire e uccidere le cellule riattivate.
Sfortunatamente, gli agenti di inversione della latenza da soli non sono in grado di ridurre le dimensioni dei serbatoi virali.
Inoltre, alcuni dei modelli di vaccino più promettenti fino ad oggi coinvolgono anticorpi neutralizzanti ampiamente (bNAbs), un raro tipo di anticorpo in grado di colpire la maggior parte delle varianti dell'HIV.
I BNAb sono stati scoperti per la prima volta in diversi controllori d'élite dell'HIV, persone che sembrano avere la capacità di sopprimere la replicazione virale senza ART e non mostrano alcuna evidenza di progressione della malattia. Alcuni di questi anticorpi specializzati, come VRC01, sono in grado di neutralizzare oltre il 95% delle varianti dell'HIV.
Attualmente, i ricercatori sui vaccini stanno tentando di stimolare la produzione di bNAb.
Uno studio del 2019 che ha coinvolto le scimmie mostra una promessa. Dopo aver ricevuto una singola iniezione di un vaccino contro l'HIV, sei delle 12 scimmie nello studio hanno sviluppato anticorpi che hanno ritardato significativamente l'infezione e, in due casi, persino l'hanno prevenuta.
Questo approccio è ancora nelle prime fasi delle sperimentazioni sull'uomo, anche se nel marzo 2020 è stato annunciato che per la prima volta gli scienziati sono stati in grado di ideare un vaccino che induce le cellule umane a generare bNAb.
Questo è uno sviluppo notevole, dopo anni di studi passati, che fino a questo punto sono stati ostacolati dalla mancanza di una risposta bNAb robusta o specifica.
Vettori dell'HIV nella terapia genica
L'HIV inattivato viene ora esplorato come un potenziale sistema di somministrazione per il trattamento di altre malattie, tra cui:
- Leucemia
- Immunodeficienza combinata grave (SCID)
- Leucodistrofia metacromatica
Trasformando l'HIV in un "vettore" non infettivo, gli scienziati ritengono di poter utilizzare il virus per fornire la codifica genetica alle cellule che l'HIV infetta preferenzialmente.
Una parola da Verywell
Comprendendo meglio il modo in cui funzionano i retrovirus, gli scienziati sono stati in grado di sviluppare nuovi farmaci.
Ma anche se ora ci sono opzioni di trattamento che in precedenza non esistevano, le migliori possibilità di una persona di vivere una vita lunga e sana con l'HIV si riducono alla diagnosi il prima possibile, tramite test regolari.
Una diagnosi precoce significa un accesso più precoce al trattamento, per non parlare della riduzione della malattia associata all'HIV e dell'aumento dell'aspettativa di vita.


.jpg)