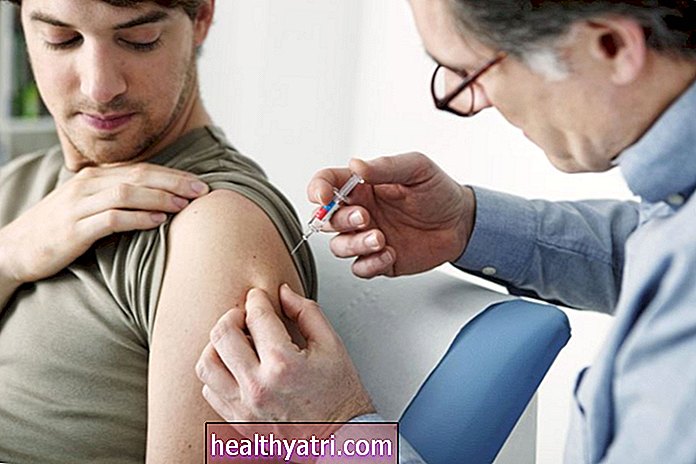
Il 27 febbraio, il vaccino di Johnson & Johnson contro il coronavirus 2019 (COVID-19) è diventato il terzo vaccino COVID-19 a ricevere l'autorizzazione per l'uso di emergenza (EUA) dalla Food and Drug Administration (FDA) statunitense.
L'azienda ha lavorato con il suo braccio farmaceutico Janssen per sviluppare il vaccino con i nomi di progetto Ensemble ed Ensemble 2. L'azienda ha arruolato partecipanti per la sua fase avanzata a settembre e ha testato il suo vaccino con due dosi diverse.
Dopo che una singola dose si è rivelata efficace negli studi clinici, Johnson & Johnson ha presentato domanda per la EUA per la singola dose. Ora il primo vaccino COVID-19 da somministrare in una dose negli Stati Uniti, è autorizzato per gli adulti dai 18 anni in su.
Immagini di Tang Ming Tung / Getty Images
Come funziona
Il vaccino di Johnson & Johnson è un vaccino monodose a base di adenovirus. Si tratta di un vaccino vettore virale che utilizza un patogeno vivo indebolito (adenovirus) come metodo di somministrazione (vettore) per il trasporto di un vaccino ricombinante per COVID-19.
I vaccini ricombinanti utilizzano un piccolo pezzo di materiale genetico del virus per innescare una risposta immunitaria. Questo materiale genetico per COVID-19 non si replica nel corpo. Un pezzo specifico del virus può essere preso di mira ei vaccini ricombinanti sono comuni e generalmente sicuri da usare in una vasta popolazione di persone, anche quelle con problemi di salute cronici o che sono immunocompromessi.
Ci possono essere alcuni inconvenienti nei vaccini ricombinanti. Un esempio è che nel tempo potrebbero essere necessari colpi di richiamo. Esempi di vaccini ricombinanti sono i vaccini pneumococcici e i vaccini per la malattia da meningococco.
La scienza alla base dei vaccini ricombinanti adenovirali vettoriali esiste da molto tempo, ma l'unico vaccino a base di adenovirus disponibile in commercio è un vaccino contro la rabbia per animali. I vaccini a base di adenovirus possono anche porre alcuni problemi in quanto l'adenovirus è così comune che il vaccino potrebbe non essere altrettanto efficace una volta somministrate le dosi di richiamo o che alcune persone potrebbero già avere l'immunità al virus utilizzato nel vaccino.
Quanto è efficace?
Johnson & Johnson ha annunciato che il suo vaccino monodose era efficace al 66% per cento nel prevenire la malattia da moderata a grave da COVID-19 e all'85% efficace nel prevenire la malattia grave. Questa efficacia nello studio di fase 3 è stata raggiunta 28 giorni dopo la vaccinazione.
Il processo ha avuto un ritardo temporaneo ad ottobre quando si è interrotto per una malattia inspiegabile, sebbene non siano stati forniti dettagli specifici su ciò che è accaduto a causa della privacy del paziente. I regolatori hanno stabilito che l'evento non era correlato al vaccino e la sperimentazione poteva riprendere in sicurezza.
L'efficacia contro l'infezione da COVID-19 da moderata a grave varia in base alla regione nello studio. Era del 72% negli Stati Uniti, del 66% in America Latina e del 57% in Sud Africa.
Il vaccino è stato anche trovato completamente protettivo contro il ricovero in ospedale e la morte e la protezione contro malattie gravi includeva più varianti di COVID-19, inclusa la variante B.1.351 trovata in Sud Africa.
Quando sarà disponibile?
Il vaccino Johnson & Johnson ha ottenuto l'autorizzazione per l'uso di emergenza dalla FDA per il suo vaccino monodose e la distribuzione è in corso.
Johnson & Johnson ha un contratto con il governo degli Stati Uniti per 100 milioni di dosi (l'equivalente di $ 10 per dose) e l'opzione di acquistare ulteriori 200 milioni di dosi.
Il governo degli Stati Uniti ha annunciato una partnership con Merck per accelerare la produzione del vaccino Johnson & Johnson. Merck riceverà fino a 268,8 milioni di dollari dalla Biomedical Advanced Research and Development Authority (BARDA) per adattare e rendere disponibili i suoi impianti di produzione per la produzione del vaccino Johnson & Johnson COVID-19.
Vaccini COVID-19: tieniti aggiornato su quali vaccini sono disponibili, chi può ottenerli e quanto sono sicuri.
I Centers for Disease Control and Prevention (CDC) stanno guidando gli sforzi di vaccinazione e tutti gli ordini di vaccini COVID-19, indipendentemente dal produttore, passeranno attraverso l'agenzia. Il CDC sta anche supervisionando la distribuzione dei vaccini.
Il Comitato consultivo per le pratiche di immunizzazione (ACIP) del CDC ha formulato raccomandazioni su come dare la priorità alle forniture di vaccini, ma può variare a seconda dello stato durante la distribuzione. Gli operatori sanitari e le persone che vivono in strutture di assistenza a lungo termine sono i primi a ricevere i vaccini e ulteriori gruppi prioritari includono lavoratori essenziali, persone di età pari o superiore a 65 anni e persone con condizioni mediche ad alto rischio.
Secondo il CDC, ci sono più di 18 milioni di operatori sanitari negli Stati Uniti e circa 1,3 milioni di americani che vivono in strutture di assistenza a lungo termine.
Il CDC ha stimato che ci vorranno diversi mesi prima che la fornitura di vaccini raggiunga la domanda.Indicazioni su chi riceverà il vaccino e su quando verranno aggiornate non appena le scorte saranno disponibili.
Gli Stati Uniti da soli hanno una popolazione di circa 330 milioni. Il presidente Biden ha annunciato il 2 marzo che potrebbero esserci sufficienti dosi di vaccino COVID-19 disponibili per tutti gli adulti statunitensi entro la fine di maggio.
Sebbene siano disponibili poche informazioni sulle specifiche di quando tutti riceveranno il vaccino e dove possono ottenerlo, i dipartimenti sanitari statali e locali coordineranno gli sforzi per distribuire le dosi dei vaccini non appena saranno disponibili. Il vaccino dovrebbe essere disponibile sia negli uffici dei medici che nei punti vendita al dettaglio come le farmacie che somministrano altri vaccini.
Quanto costa un vaccino COVID-19?
Una volta che il vaccino sarà disponibile, qualsiasi dose acquistata dal governo degli Stati Uniti sarà gratuita per i suoi cittadini. Sebbene il vaccino stesso sia gratuito, la struttura o l'agenzia che offre il vaccino può addebitare una commissione per l'amministrazione. I programmi di sanità pubblica e i piani assicurativi rimborseranno i pazienti per qualsiasi costo associato alla vaccinazione COVID-19 ea nessuno può essere negato un vaccino se non sono in grado di pagare una tassa amministrativa del vaccino.
Chi può ricevere il vaccino Johnson & Johnson?
I primi sforzi di vaccinazione per la maggior parte dei candidati al vaccino COVID-19 si stanno concentrando sulle popolazioni adulte, con opzioni di vaccino per bambini e adolescenti previste più avanti nel 2021.
Il vaccino Johnson & Johnson non fa eccezione. Il vaccino è autorizzato negli adulti di età pari o superiore a 18 anni e gli studi di fase 3 sono stati condotti su adulti di età pari o superiore a 18 anni con una rappresentanza significativa di individui di età superiore ai 60 anni.
Effetti collaterali ed eventi avversi
In ogni sperimentazione clinica, ai partecipanti viene chiesto di registrare tutte le reazioni che hanno dopo aver ricevuto un farmaco o un vaccino. Le reazioni avverse sono considerate reazioni ai farmaci direttamente causate da un vaccino, mentre un effetto collaterale è una reazione fisica a un farmaco.
Le informazioni di sicurezza iniziali rilasciate per il vaccino mostrano che le reazioni più comuni dopo la somministrazione del vaccino includevano:
- Dolore, arrossamento o gonfiore nel sito di iniezione
- Fatica
- Mal di testa
- Dolori muscolari
- Nausea
- Febbre
Le persone immunocompromesse, comprese quelle che ricevono terapie immunosoppressive, possono avere una risposta immunitaria ridotta al vaccino, secondo la FDA.
Finanziamento e sviluppo
Johnson & Johnson ha cofinanziato lo sviluppo del vaccino come parte dell'operazione Warp Speed, una partnership pubblico-privata avviata dal governo degli Stati Uniti per facilitare e accelerare lo sviluppo di un vaccino COVID-19, la produzione e la distribuzione di vaccini COVID-19 , con il finanziamento della Biomedical Advanced Research and Development Authority (BARDA), un programma del governo degli Stati Uniti volto a promuovere la produzione e la distribuzione di vaccini per combattere il COVID-19. Johnson & Johnson ha detto che $ 1 miliardo è stato investito nel progetto del vaccino sia dalla società che da BARDA.






.jpg)








.jpg)