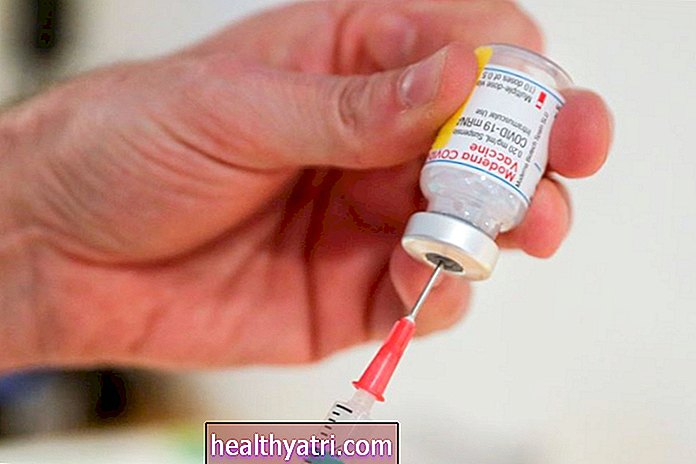
Olivier Matthys / Getty Images
Punti chiave
- Janssen Pharmaceutical Companies, una divisione di Johnson & Johnson, prevede di iniziare le sperimentazioni umane del suo vaccino COVID-19 questo mese.
- I primi partecipanti alla sperimentazione clinica saranno adulti sani.
- Il passaggio alla fase successiva degli studi clinici dipende sia dai risultati di questa fase che dalla progressione della pandemia.
Sono in corso studi clinici per tre candidati vaccini COVID-19 finanziati dagli Stati Uniti. Moderna e AstraZeneca hanno avviato sperimentazioni sull'uomo e Johnson & Johnson prevede di farlo entro la fine di luglio.
Anche con un finanziamento di oltre 2 miliardi di dollari dalla Biomedical Advanced Research and Development Authority (BARDA) del governo, ottenere un vaccino attraverso studi sull'uomo non è facile. Test su larga scala devono dimostrare che un vaccino è sicuro e può effettivamente fornire immunità contro il virus SARS-CoV-2 che causa COVID-19.
Verywell ha parlato con Jerome Custers, direttore scientifico senior della ricerca sui vaccini presso Johnson & Johnson, per scoprire cosa comporta il processo e cosa renderà le sperimentazioni umane di successo.
Marcatori di successo
Il parametro più importante in una sperimentazione umana, secondo Custers, è la sicurezza.
"Nella nostra prima sperimentazione clinica, vaccineremo adulti sani e quelle persone saranno monitorate molto rigorosamente per la sicurezza", afferma Custers. "Inoltre, stiamo cercando di vedere se il nostro vaccino è in grado di indurre una forte risposta immunitaria e produrre anticorpi contro il coronavirus".
Custers dice che gli anticorpi possono essere misurati da campioni di sangue. I ricercatori prenderanno campioni di sangue dai partecipanti alla sperimentazione prima che venga loro somministrato il vaccino, una o due settimane dopo la vaccinazione, e successivamente a intervalli regolari.
"Abbiamo dati sugli animali - scimmie, topi e criceti - che hanno confermato ciò che pensavamo di vedere e ci stanno incoraggiando a continuare in questa direzione".
Creazione e test di un vaccino
La direzione a cui si riferisce Custers è l'uso di qualcosa chiamato tecnologia AdVac. Utilizzando questa piattaforma di vaccini, gli scienziati Johnson & Johnson rimuovono un pezzo della sequenza genetica dall'adenovirus, che causa il comune raffreddore. Quindi, inseriscono il codice genetico da COVID-19.
Johnson & Johnson ha utilizzato la stessa piattaforma AdVac per sviluppare vaccini per Ebola, HIV, RSV e Zika, che combinati, sono stati testati in sicurezza su oltre 50.000 persone. Con COVID-19, tuttavia, l'azienda sta cercando di farlo su una scala molto più ampia e con una tempistica molto più abbreviata.
"Un miliardo di vaccini è ancora l'obiettivo", dice Custers.
Mentre i primi studi clinici sull'uomo erano inizialmente previsti per settembre, la società ha annunciato il 10 giugno che li avrebbe sospesi fino alla seconda metà di luglio. Questa fase, considerata una sperimentazione clinica di Fase 1 / 2a, coinvolgerà 1.045 volontari. In genere, questo richiede diversi mesi o anni. Ma Johnson & Johnson sta già guardando avanti alla Fase 3, in cui Moderna e AstraZeneca prevedono di entrare quest'estate.
L'inizio degli studi clinici di Fase 3 è subordinato ai buoni risultati della Fase 1 / 2a.
"Stiamo pensando che le prove di Fase 3 includeranno diverse decine di migliaia di persone", afferma Custers. “Ma ciò dipenderà in gran parte da come si svilupperà la pandemia. Il tasso di incidenti di infezione sta diminuendo. "
Attualmente, gli studi clinici di fase 1 / 2a sono previsti negli Stati Uniti e in Belgio. Il Belgio ha registrato un calo costante dei casi confermati di COVID-19 da aprile, quando i casi hanno raggiunto il picco di oltre 2.000 in un solo giorno. Per tutto il mese di giugno, i nuovi casi si sono aggirati intorno ai 100 al giorno.
"Naturalmente, siamo felici che stia accadendo, ma renderà anche molto più difficile dimostrare che il vaccino può prevenire l'infezione", afferma Custers. "Hai bisogno di un certo tasso di incidenza per poterlo fare."
Custers afferma che, se necessario, Johnson & Johnson potrebbe spostare i test in aree in cui i tassi di infezione sono ancora alti.
"È molto difficile valutare come sarà la situazione tra un paio di mesi quando avremo effettivamente bisogno di decidere", dice Custers. "Stiamo monitorando la situazione. Pensiamo che sarà un potenziale problema per tutti i vaccini COVID-19 in fase di sviluppo ".
Vaccini COVID-19: tieniti aggiornato su quali vaccini sono disponibili, chi può ottenerli e quanto sono sicuri.
Imparare da altri vaccini
Oltre ai vaccini che ricevono finanziamenti BARDA negli Stati Uniti, ci sono circa 140 vaccini COVID-19 in fase di sviluppo in tutto il mondo. Custers spiega che la corsa per un vaccino non è una competizione, è una collaborazione.
"Nessuno sa chi avrà successo, quindi è importante che il mondo abbia più tiri in porta, come tendiamo a dire", dice. "È importante anche perché impariamo gli uni dagli altri. Siamo tutti in fasi diverse e abbiamo approcci leggermente diversi. I dati che generiamo, in dati preclinici, studi sugli animali e studi clinici, consentiranno a tutti noi di muoverci il più rapidamente possibile ".
Sfide cronologiche
Mentre Johnson & Johnson e altre aziende biofarmaceutiche stanno lavorando il più rapidamente possibile per creare un vaccino utilizzabile, è ancora impossibile fornire una tempistica definitiva.
Custers dice che una serie di fattori influenzano il tempismo. "I vaccini attualmente in fase di sviluppo avranno successo?" lui dice. "Saremo in grado di dimostrare che quei vaccini funzionano? L'incidenza del COVID-19 da qualche parte nel mondo è abbastanza alta da essere in grado di dimostrare che il vaccino può proteggere sufficientemente le persone?"
Anche se entrambe le risposte sono sì, la scala della produzione è un'altra sfida.
"Dobbiamo fare una quantità sufficiente di vaccino", dice Custers. "All'inizio, non ci sarà abbastanza vaccino per offrirlo al grande pubblico. Immagino che gli operatori sanitari e le persone a maggior rischio di contrarre COVID-19 riceveranno prima il vaccino. Non dipende da noi come azienda ".
Custers afferma che l'implementazione di un vaccino, supponendo che si sia dimostrato sicuro ed efficace, dipende da quando Johnson & Johnson riceve l'autorizzazione all'uso di emergenza a livello governativo, come dalla Food and Drug Administration.
Custers afferma che il suo team sta lavorando duramente per soddisfare queste richieste di fornitura.
“Stiamo facendo le cose in parallelo. La produzione è in corso e stiamo aumentando la scala per essere in grado di preparare il maggior numero di dosi di vaccino il prima possibile ", afferma. "Di solito, lo fai solo quando sai che il vaccino funziona."
Dice che mentre molto rimane incerto, Johnson & Johnson è ottimista sul loro candidato vaccino.
"È molto gratificante e motivante lavorare su questo vaccino ed essere in grado di contribuire con qualcosa", dice. "È un'opportunità che capita una volta nella vita, si spera."