wera Rodsawang / Getty Images
Punti chiave
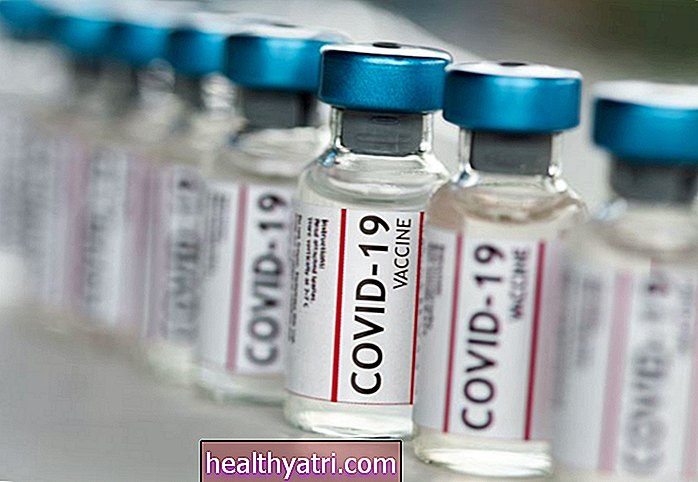
- Un nuovo vaccino a RNA messaggero (mRNA) è diventato il primo vaccino COVID-19 autorizzato per l'uso di emergenza negli Stati Uniti
- I ricercatori stanno lavorando su 10 diversi modelli di vaccini esistenti per creare vaccini COVID-19
- Un vaccino deve essere efficace almeno al 70% per sradicare COVID-19
- Rintracciare rapidamente un vaccino significa aggirare le misure di salvaguardia
La corsa per trovare un vaccino sicuro ed efficace per COVID-19 (malattia da coronavirus 2019) non ha precedenti nella storia medica moderna. Non dalla pandemia di AIDS se gli anni '80 e '90 hanno visto scienziati, governi e imprese si uniscono in uno sforzo coordinato per condividere conoscenze e risorse che un giorno potrebbero portare allo sviluppo di un vaccino completamente protettivo.
Come per la pandemia di AIDS, c'è molto che gli scienziati devono imparare sul virus.
Ma c'è speranza. A dicembre 2020, c'erano non meno di 233 vaccini candidati in fase di sviluppo attivo in Nord America, Europa e Asia, con l'obiettivo di introdurne almeno uno sul mercato entro il 2021.
L'11 dicembre la Food and Drug Administration (FDA) ha concesso l'autorizzazione all'uso di emergenza per un candidato vaccino COVID-19 co-sviluppato da Pfizer e BioNTech.Questo uso di emergenza è approvato per persone di età pari o superiore a 16 anni. Un altro candidato vaccino COVID-19 di Moderna ha ottenuto l'autorizzazione all'uso di emergenza il 18 dicembre. Entrambi i vaccini sono nuovi vaccini a RNA messaggero (mRNA) che trasportano istruzioni genetiche affinché le nostre cellule immunitarie facciano parte di una proteina che innesca una risposta immunitaria a COVID. -19.
Perché questo è importante
Per quanto scoraggianti possano sembrare le sfide, un vaccino rimane il modo più efficace per prevenire i blocchi globali e le misure di allontanamento sociale che hanno definito la pandemia iniziale di COVID-19.
Obiettivi e sfide
La stessa sequenza temporale pone enormi sfide. Dato che i vaccini impiegano in media 10,71 anni per svilupparsi dall'inizio della ricerca preclinica alle approvazioni normative finali, gli scienziati hanno il compito di comprimere la sequenza temporale in un modo che è in gran parte inaudito nella ricerca sui vaccini.
Affinché un vaccino sia considerato praticabile, deve essere sicuro, poco costoso, stabile, facilmente fabbricato su scala di produzione e facilmente somministrato al maggior numero possibile dei 7,8 miliardi di persone che vivono sul pianeta.
Allo stesso tempo, se un vaccino vuole porre fine alla pandemia, dovrà avere un alto livello di efficacia, anche superiore a quello del vaccino antinfluenzale. Qualsiasi cosa al di sotto di questo può temperare la diffusione delle infezioni, ma non fermarle.
Solo il 6% dei vaccini in fase di sviluppo proviene dalla ricerca preclinica fino al rilascio sul mercato.
Efficacia del vaccino
Secondo l'Organizzazione mondiale della sanità (OMS), affinché un vaccino possa sradicare completamente il COVID-19, deve essere efficace non meno del 70% su base di popolazione e fornire una protezione duratura per almeno un anno. A questo livello, il virus sarebbe meno in grado di mutare mentre passa da persona a persona e più probabilità di generare immunità di gregge (in cui ampi settori della popolazione sviluppano resistenza immunitaria al virus).
Questi parametri di riferimento sono incredibilmente ambiziosi, ma non impossibili.
Con un'efficacia del 60%, l'OMS sostiene che si verificherebbero ancora focolai e che l'immunità della mandria non si svilupperebbe in modo abbastanza aggressivo da porre fine alla pandemia.
Un vaccino COVID-19 con un'efficacia del 50%, sebbene benefico per le persone ad alto rischio, non impedirebbe le epidemie né ridurrebbe lo stress sui sistemi sanitari in prima linea in caso di epidemia.
L'efficacia del vaccino antinfluenzale, ad esempio, è stata inferiore al 45% durante la stagione influenzale 2019-2020, secondo i Centers for Disease Control and Prevention (CDC). Alcuni dei singoli componenti del vaccino erano efficaci solo al 37%.
Vaccini mRNA per COVID-19
Pfizer ha annunciato il 18 novembre che la sua sperimentazione di fase III sul vaccino ha dimostrato un'efficacia del 95% contro COVID-19. Moderna ha annunciato il 30 novembre che la sperimentazione di fase III del vaccino ha mostrato un'efficacia del 94% contro COVID-19 in generale e anche del 100% contro malattie gravi La revisione tra pari è ancora in sospeso per queste prove.
Le autorità sanitarie possono approvare un vaccino con efficacia non ottimale se i benefici (in particolare per gli anziani e i poveri) superano i rischi.
Costo
Un vaccino non può essere considerato praticabile se non è conveniente.
A differenza del vaccino antinfluenzale, prodotto in serie iniettando il virus nelle uova di gallina, né COVID-19 né alcuno dei suoi cugini del coronavirus (come SARS e MERS) possono essere riprodotti nelle uova. Pertanto, è necessaria una tecnologia di produzione completamente nuova per abbinare il volume di produzione del vaccino antinfluenzale annuale, di cui oltre 190 milioni di dosi vengono fornite negli Stati Uniti ogni anno.
Nuovi vaccini genetici, compresi i candidati vaccini Pfizer-BioNTech e Moderna, vengono sviluppati in provette o serbatoi. Non hanno bisogno di essere coltivati in uova o cellule, il che consente di risparmiare tempo e costi di sviluppo, anche se questa è la prima volta che vengono prodotti in serie, quindi i costi completi e molte logistiche sono ancora sconosciute.
Gli Stati Uniti hanno contratti per l'acquisto di dosi dei candidati vaccini a mRNA da Pfizer-BioNTech e Moderna, ma i costi e l'accessibilità di questi vaccini e di altri in molti paesi del mondo sono ancora indeterminati.
Il governo degli Stati Uniti ha un contratto con Pfizer e BioNTech per un ordine iniziale di 100 milioni di dosi per 1,95 miliardi di dollari e il diritto di acquisire fino a 500 milioni di dosi aggiuntive. Coloro che ricevono il vaccino lo ottengono gratuitamente Il vaccino ha anche ricevuto l'autorizzazione per l'uso di emergenza nel Regno Unito, Bahrain, Arabia Saudita, Canada e Messico.
Il governo federale ha un contratto da 1,5 miliardi di dollari con Moderna per 100 milioni di dosi del vaccino e l'opzione per acquisire ulteriori 400 milioni di dosi (ne ha già richiesti altri 100 milioni). Ha anche contribuito a finanziare il suo sviluppo con un contratto da 955 milioni di dollari, portando il totale iniziale a 2,48 miliardi di dollari. Se riceve l'autorizzazione di emergenza, sarà anche dato gratuitamente alle persone negli Stati Uniti.
Distribuzione
Dopo che i vaccini COVID-19 sono stati sviluppati, la sfida successiva è distribuirli in modo equo, soprattutto se la capacità di produzione è limitata. Ciò richiede un'ampia ricerca epidemiologica per determinare quali popolazioni sono a maggior rischio di malattia e morte.
Al fine di eludere queste preoccupazioni, alcuni esperti hanno raccomandato che i finanziamenti siano diretti a modelli di vaccini collaudati che hanno maggiori probabilità di essere scalabili piuttosto che a quelli sperimentali che potrebbero richiedere miliardi di dollari in investimenti strutturali prima che la prima assegnazione del vaccino sia pari. prodotto.
Tuttavia, sono stati fatti importanti investimenti su quelli sperimentali, anche se pongono sfide per la distribuzione di massa, compresi i potenziali costi e requisiti di temperatura ultra-fredda per il vaccino Pfizer-BioNTech che necessita di congelatori specializzati.
Pfizer e BioNTech prevedono una produzione globale fino a 50 milioni di dosi nel 2020 e fino a 1,3 miliardi di dosi entro la fine del 2021. Moderna prevede una produzione di circa 20 milioni di dosi pronte per la spedizione negli Stati Uniti entro la fine del 2020 e una produzione globale da 500 milioni a 1 miliardo di dosi nel 2021.
Dilemmi etici
Il monitoraggio rapido di un vaccino riduce al minimo alcuni dei controlli e degli equilibri progettati per mantenere le persone al sicuro. Ciò non significa che ciò sia impossibile. Richiede semplicemente una maggiore supervisione da parte di organi di controllo normativi come l'OMS, il National Institutes of Health (NIH), l'Agenzia europea per i medicinali (EMA) e la Food and Drug Administration (CFDA) cinese, tra gli altri, per garantire che la ricerca sia condotta in sicurezza ed eticamente.
Anche con una maggiore supervisione normativa, la corsa per produrre un vaccino pronto per il mercato entro due anni ha sollevato preoccupazioni tra gli esperti di etica che sostengono che non è possibile sviluppare rapidamente un vaccinoein modo sicuro.
Gli "studi di sfida", ad esempio, coinvolgono il reclutamento di giovani adulti sani, precedentemente non infetti che sono direttamente esposti a COVID-19 dopo aver subito la vaccinazione con il vaccino candidato. Se un vaccino di sfida si rivela sicuro ed efficace in questo a basso rischio gruppo, il passo successivo sarebbe quello di reclutare adulti ad alto rischio in uno studio tradizionale in doppio cieco. Mentre sfide come questa vengono utilizzate con malattie meno mortali, come l'influenza, esporre deliberatamente le persone a COVID-19 è considerevolmente più rischioso.
Mentre la ricerca sul COVID-19 si sposta da studi preclinici a sperimentazioni umane più ampie, dilemmi come questi eserciteranno pressioni sui regolatori per decidere quali rischi in questa nuova frontiera sono "accettabili" e quali no.
Dove iniziare
Gli scienziati non iniziano da zero quando sviluppano i loro modelli di vaccino COVID-19 (chiamati piattaforme). Non esistono solo vaccini efficaci basati su virus correlati, ma anche sperimentali che hanno dimostrato una protezione parziale contro i coronavirus come MERS e SARS.
COVID-19 appartiene a un ampio gruppo di virus chiamati virus RNA che includono Ebola, epatite C, HIV, influenza, morbillo, rabbia e una miriade di altre malattie infettive. Questi sono ulteriormente suddivisi in:
- Virus RNA del gruppo IV: includono coronavirus, virus dell'epatite, flavivirus (associati a febbre gialla e febbre del Nilo occidentale), poliovirus e rinovirus (uno dei numerosi virus del raffreddore comuni
- Coronaviridae: una famiglia di virus RNA del gruppo IV che include quattro ceppi di coronavirus legati al comune raffreddore e tre che causano gravi malattie respiratorie (MERS, SARS e COVID-19)
La conoscenza di questi virus, per quanto scarsa, può fornire ai ricercatori le prove necessarie per costruire e testare le loro piattaforme. Anche se una piattaforma fallisce, può indirizzare i ricercatori nella direzione di quelle più praticabili.
Anche tra i tanti virus a RNA del gruppo IV, solo una manciata di vaccini (poliomielite, rosolia, epatite A, epatite B) sono stati sviluppati dal primo vaccino contro la febbre gialla nel 1937. Finora non ci sono vaccini per i coronavirus che sono completamente approvati e concessi in licenza negli Stati Uniti.
Modelli per lo sviluppo di vaccini
La corsa per trovare un vaccino COVID-19 efficace è coordinata in gran parte dall'OMS e da partner globali come la Coalition for Epidemic Preparedness Innovations (CEPI) di recente formazione. Il ruolo di queste organizzazioni è quello di supervisionare il panorama della ricerca in modo che le risorse possano essere indirizzate ai candidati più promettenti.
CEPI ha delineato le varie piattaforme disponibili su cui costruire COVID-19. Alcuni sono modelli aggiornati basati sui vaccini antipolio Salk e Sabin degli anni '50 e '60. Altri sono vaccini di nuova generazione che si basano sull'ingegneria genetica o su nuovi sistemi di somministrazione (chiamati vettori) per colpire le cellule respiratorie.
vaccini proteici
Ci sono vantaggi e svantaggi per ciascuna delle piattaforme proposte. Alcuni dei tipi di vaccino sono facilmente fabbricati su una scala di produzione ma sono più generalizzati nella loro risposta (e, quindi, meno probabilità di raggiungere i tassi di efficacia necessari per porre fine alla pandemia). Altri modelli più recenti possono suscitare una risposta più forte, ma poco si sa su quanto potrebbe costare il vaccino o se può essere prodotto su scala globale.
Delle 10 piattaforme vaccinali delineate da CEPI, cinque non hanno mai prodotto un vaccino praticabile negli esseri umani. Anche così, alcuni (come la piattaforma del vaccino a DNA) hanno creato vaccini efficaci per gli animali.
Processo di sviluppo del vaccino
Anche se le fasi di sviluppo del vaccino sono compresse, il processo con cui vengono approvati i vaccini COVID-19 rimarrà più o meno lo stesso. Le fasi possono essere suddivise come segue:
- Fase preclinica
- Sviluppo clinico
- Revisione e approvazione normativa
- Produzione
- Controllo di qualità
La fase preclinica è il periodo durante il quale i ricercatori raccolgono dati di fattibilità e sicurezza, insieme alle prove di studi precedenti, da sottoporre alle autorità di regolamentazione governative per l'approvazione dei test. Negli Stati Uniti, la FDA supervisiona questo processo. Altri paesi o regioni hanno i propri organismi di regolamentazione.
Lo sviluppo clinico è la fase durante la quale viene condotta la ricerca effettiva sugli esseri umani. Ci sono quattro fasi:
- La fase I mira a trovare la dose migliore con il minor numero di effetti collaterali. Il vaccino sarà testato in un piccolo gruppo di meno di 100 partecipanti. Circa il 70% dei vaccini supera questa fase iniziale.
- La fase II estende i test a diverse centinaia di partecipanti in base alla dose considerata sicura. La ripartizione dei partecipanti corrisponderà alla demografia generale delle persone a rischio di COVID-19. Circa un terzo dei candidati della Fase II arriverà alla Fase III.
- La fase III coinvolge migliaia di partecipanti in più siti che vengono selezionati casualmente per ottenere il vero vaccino o un placebo. Questi studi sono tipicamente in doppio cieco in modo che né i ricercatori né i partecipanti sappiano quale vaccino viene somministrato. Questa è la fase in cui la maggior parte dei vaccini fallisce.
- La fase IV si svolge dopo che il vaccino è stato approvato e continua per diversi anni per valutare l'efficacia e la sicurezza del vaccino nel mondo reale. Questa fase è anche nota come "sorveglianza post-marketing".
Vaccini COVID-19: tieniti aggiornato su quali vaccini sono disponibili, chi può ottenerli e quanto sono sicuri.
Tempistica
Per quanto semplice sia il processo, ci sono molte cose oltre al fallimento del vaccino che possono aggiungere mesi o anni al processo. Tra questi c'è il tempismo. Sebbene un candidato vaccino dovrebbe idealmente essere testato durante un'epidemia attiva, può essere difficile sapere dove o quando potrebbe verificarsi.
Anche in aree duramente colpite come New York City e Wuhan, in Cina, dove un'ulteriore epidemia sembra imminente, i funzionari della sanità pubblica possono intervenire per prevenire le malattie con misure come richiedere alle persone di autoisolarsi di nuovo. Questo è importante per mantenere le persone in buona salute, ma può estendere le sperimentazioni sui vaccini per un'intera stagione o anno.
Candidati al vaccino nella pipeline
A dicembre 2020, 56 candidati vaccini sono stati approvati per la ricerca clinica, mentre oltre 165 sono nelle fasi precliniche in attesa di approvazione normativa.
Tra le piattaforme approvate per i test, i vaccini inattivati sono tra i più comuni. Ciò include subunità proteiche, che utilizzano antigeni (componenti che stimolano meglio il sistema immunitario) invece dell'intero virus, e vaccini inattivati a cellule intere, alcuni dei quali utilizzano agenti "stimolanti" come l'alluminio per aumentare la risposta anticorpale.
Anche i vaccini a RNA e DNA sono ben rappresentati, così come i vaccini con vettori che utilizzano virus del raffreddore disattivati per trasportare gli agenti vaccinali direttamente alle cellule.
Ulteriori piattaforme includono particelle simili a virus, vaccini con vettori combinati con cellule presentanti l'antigene e un vaccino vivo attenuato che utilizza una forma viva indebolita di COVID-19 per stimolare una risposta immunitaria.
(Regno Unito)
(Cina)
(Stati Uniti)
(Stati Uniti)
(Stati Uniti)
(Cina)
(Cina)
(Cina)
(Stati Uniti)
(Cina)
(Stati Uniti)