Rosley Majid / EyeEm / Getty Images
Punti chiave
- La FDA ha rilasciato l'autorizzazione all'uso di emergenza per gli anticorpi monoclonali di Regeneron - casirivimab e imdevimab - per il trattamento del COVID-19.
- Il trattamento è autorizzato solo per le persone con infezioni da COVID-19 da lievi a moderate, non per le persone ricoverate in ospedale.
- Gli anticorpi devono essere somministrati insieme tramite IV.
- Il presidente Trump ha ricevuto questi anticorpi durante la sua infezione da COVID-19.
Venerdì 21 novembre, la Food and Drug Administration (FDA) ha autorizzato l'uso del cocktail di anticorpi monoclonali di Regeneron per il trattamento del COVID-19. Il farmaco, denominato REGN-COV2, è lo stesso che il presidente Trump ha ricevuto dopo la diagnosi di COVID-19 all'inizio di ottobre.
Mentre il presidente Trump è stato ricoverato in ospedale per il suo caso di COVID-19, la recente autorizzazione per l'uso di emergenza della FDA (EUA) non è destinata alle persone già in ospedale con la malattia o che ricevono ossigenoterapia a causa di essa. Secondo la FDA, gli anticorpi sono attualmente autorizzati per il trattamento del COVID-19 da lieve a moderato e possono essere somministrati a:
- Adulti, compresi gli adulti di età superiore ai 65 anni con condizioni croniche
- Pazienti pediatrici di età pari o superiore a 12 anni che pesano almeno 40 chilogrammi (88 libbre)
Per essere idonei al trattamento REGN-COV2, la FDA afferma che i pazienti devono avere un SARS-CoV-2 positivo, il virus che causa il COVID-19, testare ed essere ad alto rischio di progredire a COVID-19 grave.
Un'autorizzazione all'uso di emergenza è diversa da un'approvazione.La FDA emette un EUA quando ci sono prove scientifiche sufficienti per dimostrare che un farmaco ha più benefici che rischi in una situazione di emergenza.
Cosa c'è nella droga?
Il cocktail di anticorpi di Regeneron è costituito da due diversi anticorpi monoclonali, casirivimab e imdevimab. La FDA EUA richiede che entrambi siano somministrati insieme tramite infusione endovenosa (IV).
Un anticorpo monoclonale è un clone prodotto in laboratorio di una specifica cellula immunitaria madre destinata a combattere le infezioni nel corpo. Casirivimab e imdevimab agiscono impedendo alla proteina spike di SARS-CoV-2 virtus di legarsi ai recettori nelle cellule umane.
Per produrre questi anticorpi in un laboratorio, gli scienziati di Regneron hanno valutato gli anticorpi di persone che si erano riprese da COVID-19 e gli anticorpi umani prodotti dai topi. Ti stai chiedendo come funziona? Gli scienziati usano topi che sono stati geneticamente modificati per avere un sistema immunitario umano.
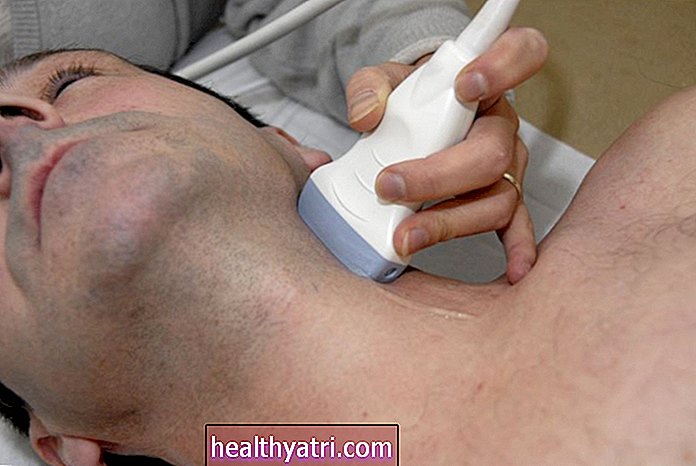
Come si ottiene?
L'autorizzazione della FDA dice che REGN-COV2 dovrebbe essere somministrato attraverso una flebo, ma non è indicato per i pazienti COVID-19 ospedalizzati. Questo pone la domanda: come potresti ricevere una flebo al di fuori di un ambiente ospedaliero?
"L'indicazione di somministrare questi anticorpi a individui che non sono / devono ancora essere ricoverati in ospedale presenta certamente alcune sfide logistiche", dice a Verywell via e-mail Aaron Emmel, PharmD, MHA, BCPS, fondatore e direttore di PharmacyTechScholar.com. Dice che idealmente, la combinazione casirivimab / imdevimab potrebbe essere somministrata direttamente nello studio del tuo medico di base. Tuttavia, la maggior parte degli uffici PCP non è configurata per fornire la terapia infusionale IV.
"Ciò richiede politiche, procedure e personale sanitario qualificato", afferma. "Ora è un momento particolarmente difficile per queste pratiche per stabilire questi processi quando così tante pratiche sono state interrotte da COVID-19".
In definitiva, il modo in cui vengono somministrati gli anticorpi dipenderà probabilmente da dove vivi.
"Penso che vedrete una significativa disparità nel luogo in cui questi farmaci vengono somministrati, basata principalmente su come sono progettati gli ecosistemi sanitari locali in tutto il paese", dice Emmel. "Nelle aree con sistemi sanitari ben consolidati, è possibile che si verifichi uno sforzo coordinato per indirizzare i pazienti a una struttura locale di cure urgenti o a un centro di infusione ambulatoriale ospedaliero per ricevere le cure".
Aaron Emmel, PharmD, MHA, BCPS
Vedrai una disparità significativa nel luogo in cui questi farmaci vengono somministrati in base principalmente al modo in cui sono progettati gli ecosistemi sanitari locali in tutto il paese.
- Aaron Emmel, PharmD, MHA, BCPSEmmel prevede che l'uso di trattamenti con anticorpi nelle aree più rurali sarà molto diverso.
"Potresti vedere una minore diffusione di questi trattamenti a causa delle sfide logistiche, o più fornitori che indirizzano i pazienti al pronto soccorso", dice.
Nel caso in cui i pazienti con sintomi COVID-19 da lievi a moderati vengano inviati in ospedale per ricevere un trattamento con anticorpi, Jason Reed, PharmD, afferma che è molto probabile che vengano inviati alle strutture ospedaliere per il trattamento delle infusioni.
"Queste strutture sono più adatte per trattare questo tipo di anticorpi monoclonali che devono essere accuratamente miscelati e maneggiati delicatamente durante la somministrazione", dice Reed, fondatore di BestRxForSavings.com, a Verywell via e-mail. "L'attrezzatura necessaria è già presente nei centri di trattamento delle infusioni. Molti pazienti ambulatoriali entrano già in queste strutture e possono essere facilmente separati dagli altri".
Reed aggiunge che quasi tutti gli ospedali hanno una sorta di struttura per il trattamento delle infusioni. "Alcuni ospedali possiedono più di un centro di trattamento di infusione e molti hanno siti che si trovano nella comunità e non direttamente nel campus dell'ospedale", dice.
In alcuni casi, gli infermieri di viaggio possono essere in grado di somministrare infusioni IV a casa dei pazienti. "Questa è una buona opzione, soprattutto per qualcuno che ha una COIVD-19 lieve o moderata e ha bisogno di isolarsi comunque", dice Reed.
Quanto è efficace?
I dati mostrano che la combinazione di casirivimab e imdevimab può ridurre la carica virale, la quantità di SARS-CoV-2 che circola nel sangue di una persona. Uno studio clinico su 799 adulti non ospedalizzati con sintomi COVID-19 da lievi a moderati ha mostrato che il trattamento con REGN-COV2 porta a una maggiore riduzione della carica virale dopo sette giorni rispetto al trattamento con un placebo.
Tra i pazienti considerati ad alto rischio di progressione della malattia, solo il 3% delle persone trattate con REGN-COV2 è stato ricoverato in ospedale o si è recato al pronto soccorso, rispetto al 9% delle persone trattate con un placebo.









.jpg)






.jpg)